使用温度梯度的引物优化试验方案
qPCR条件优化
QPCR 条件的优化对于制定稳健的检测方案非常重要。优化不佳的表现是重复样本之间缺乏再现性,以及检测低效且不灵敏。两种主要优化方法是优化引物浓度和/或退火温度。
测定优化的一种方法是通过在一系列退火温度下测试含有固定引物浓度的相同反应物来确定引物的最佳退火温度(Ta)。如果有带温度梯度仪的qPCR仪器可用,即可实现这种优化方法。在本实验方案所述的款式中,引物的终浓度为450nM,梯度仪的梯度为X轴,所有的列经均受相同的Ta(即12个不同的温度)。在其他仪器中,梯度沿着列向下,所有列具有相同的Ta(即8个不同的温度)。以下实验方案适用于两种仪器的任何一种,但需要进行相应的微调。
设备
- 具有集成式梯度仪控制功能的定量PCR仪
- PCR设置的层流罩(选购件)
试剂
耗材
- 无菌过滤器移液管吸头
- 无菌 1.5 mL 螺旋盖微量离心管 (CLS430909)
- PCR管和PCR板,选择一种以匹配所需格式:
• 单个独立的薄壁200μL PCR管(Z374873或P3114)
• 孔板
- 96孔板(Z374903)
- 384孔板(Z374911)
• 孔板密封
- ThermalSeal RTS™ 封膜 (Z734438)
- ThermalSeal RT2RR™ 封膜 (Z722553)
本方案注意事项
- 使用随机引发或oligo-dT引发方法产生cDNA,并以1:10稀释备用,但也可以使用任何合适的替代模板。
- 所有反应均一式两份作为技术重复。
- 如果使用PCR板,请按照板示意图(例如图P14-19所示)进行,以确保反应混合物样品
和对照被添加到正确的孔中。
方法
1. 根据表P14-35制备56个反应的预混合物。混合均匀,避免气泡。
2. 将步骤1中的448 μL预混合物(即一半)移入单独的管中,以设置无模板对照(NTC)
反应。
3. 将112 μL模板添加到步骤2中剩余的预混合物中。将模板预混合物置于冰上。
4. 将112 μL水添加到步骤2的另一半中。将NTC预混合物置于冰上。
5. 将步骤3中的20 μL模板预混合物等分添加到两行标记为GOI的PCR板孔中。
6. 将步骤4中的20 μL NTC预混合物等分添加到两行标记为NTC的PCR板孔中。
7. 给板盖上盖子并贴好标签。(确保标签不会遮挡仪器的激发/检测光路。)
8. 根据以下三步方案操作反应
(说明:这些条件是对快速循环实验方案的),确保退火温度
定义在适合引物的最低和最高温度(示例显示为
54-70°C)之间的梯度上。重复执行第1-3步40次。扩增后运行标准解离曲线。
说明:使用标准解离曲线实验方案(数据收集)。
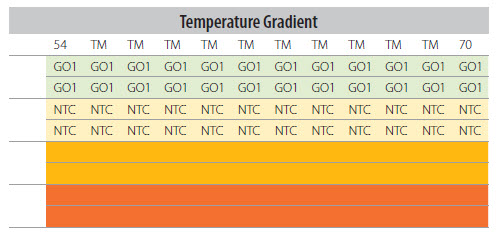
图 P14-19.每个列用相同Ta的Ta优化所使用的板布局。
注意:样品和对照在温度梯度上的分布。如果仪器的温度梯度在板柱上垂直向下变化,则需要相应地重新安排样品和对照的布局。
材料
如要继续阅读,请登录或创建帐户。
暂无帐户?