Manufacturing Strategies for mRNA Vaccines and Therapeutics
With a compressed timeframe from development to clinic, mRNA technology offers promise, not only as a fast and effective agent to respond to infectious disease outbreaks, but also for development of novel therapeutics to address diseases with unmet needs. mRNA technologies offer multiple benefits: excellent safety profile, a high degree of versatility, and a templated manufacturing process.
With the early success of mRNA vaccines, today’s mRNA manufacturers are looking to improve the efficiency and productivity of their production processes by improving mRNA stability and by implementing strategies that improve pDNA and mRNA purification and scale up to GMP production.
View all of our products and services for mRNA development and manufacturing.
Section Overview
Considerations for mRNA Manufacturing
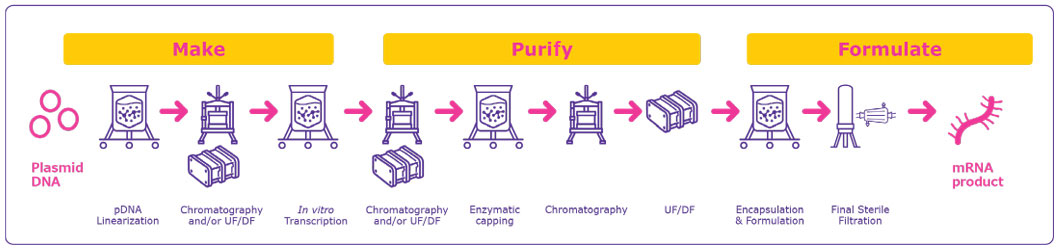
Manufacturing of mRNA vaccines and therapeutics of mRNA vaccines and therapeutics typically follows a templated process (Figure 1). This simplified manufacturing template uses the same reaction materials for any target and enables mRNA manufacturers to produce new target molecules with minimal process adaptations.
Several key decisions have an outsize impact on the process, yield and quality of the final mRNA product, and one of these is the quality of the process chemicals and raw materials. Particularly during in-vitro transcription and downstream purification, the mRNA is unprotected and at high risk for enzymatic degradation. Using high quality chemicals that are tested for the absence of endonuclease activity minimizes risk of RNase-induced degradation and improves mRNA stability throughout purification and formulation of the mRNA drug product.
This webpage will help you navigate these and other challenges, by providing information on our comprehensive, integrated solutions designed to streamline your mRNA manufacturing. Our brochure "Process chemicals for mRNA drug manufacturing" provides the details you need to make informed choices.
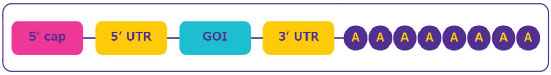
Figure 2.mRNA structure.
- Cap region at the 5’ end of the sequence: Essential for mRNA maturation, recognition by the ribosome for an efficient protein translation, and protection from nuclease digestion for improved stability.
- Untranslated regions (UTRs) at the upstream and downstream domains of the mRNA coding region: Regulating mRNA translation, localization and stability; can be utilized to improve protein expression efficiency.
- Open reading frame or coding sequence region: Contains the gene of interest (GOI).
- Poly(A) tail: Crucial for protein translation and mRNA stability by preventing digestion by 3’ exonuclease.
Making mRNA
Production of mRNA-based therapeutics and vaccines begins with a plasmid DNA (pDNA) template that is then linearized and transcribed into mRNA.
- pDNA production: The pDNA template contains a DNA-dependent RNA polymerase promoter and the sequence for the mRNA construct. The pDNA is amplified in bacterial cells which are then harvested and lysed to release the circular pDNA. This lysate is extremely viscous as it contains the pDNA and other large, negatively charged impurities such as RNA, genomic DNA and endotoxins from the bacterial cells which makes purification challenging.
- pDNA purification: Purification of the pDNA template from impurities should maximize separation while minimizing the potential of mechanical damage to the plasmid template. Purified, circular pDNA is then linearized to avoid transcriptional readthrough events that may generate undesired mRNA sequence variants that would need to be removed.1 This linearized pDNA template is further purified to remove impurities such as the restriction enzyme used for linearization, bovine serum albumin (BSA), DNA fragments, and endotoxins. As the pDNA template is typically produced in bacterial cells, endotoxin impurities are a critical impurity that impact subsequent purification steps. Detergents such as Deviron® C16 detergent can be used to effectively remove endotoxins and are a sustainable, biodegradable and REACH compliant alternative to traditional detergents.2
There are marked differences in the approach to pDNA purification at lab and GMP production scale. Lab-scale processes often use solvent extraction techniques to separate pDNA from other components, but handling and disposal of these chemicals at large scale can be challenging. By contrast, GMP production environments typically use tangential flow filtration (TFF) and chromatography for efficient impurity removal.
In-vitro transcription (IVT): The linearized and purified pDNA, is then transcribed into mRNA in an enzymatic reaction.
- Critical components for in-vitro transcription include the RNA polymerase, which catalyzes the transcription of DNA into mRNA; ribonucleoside triphosphates (rNTPs) which serve as building blocks of the mRNA; inorganic pyrophosphatase (IPP) which enhances mRNA yield; and RNase inhibitors, which prevent against RNA degradation. The transcription buffer typically contains dithiothreitol (DTT) to reduce disulfide bonds and inhibit RNase activity, while spermidine is included to improve transcription efficiency and stabilize nucleic acids. To minimize the risk of enzymatic degradation in this critical process step, it is essential to select chemicals that have been tested for the absence of endonuclease activity. For a comprehensive overview of our high-quality chemicals and excipients, including a broad portfolio of endonuclease-free products, access our brochure “Process chemicals for mRNA drug manufacturing”.
- Monitoring transcription: Critical process parameters (CPPs) should be monitored during the IVT reaction to control critical quality attributes (CQAs) and assure optimal processing. Effective monitoring enables more controlled manufacturing and faster responses to process variability.
Capping: Following transcription, a 5’ cap structure is added to the mRNA transcript to improve stability and transduction in the host cell. The cap can be added in two ways:
- Co-transcriptional capping: performed during the IVT step. However, efficiency and yield are low, and this approach can generate non-capped impurities due to wrong binding or reverse incorporation.
- Enzymatic capping (or post-translational capping) is performed after mRNA purification. This approach usually uses a capping enzyme to add the cap to the purified mRNA. While this approach is more efficient, it is more expensive and is an extra processing step following purification.
Purifying mRNA
Following the in-vitro transcription, mRNA is purified from the impurities and materials used in the previous steps including endotoxins, immunogenic double stranded RNA (dsRNA), residual DNA template, RNA polymerase and elemental impurities. Several options are available for mRNA purification and removal of residual DNA.
Chromatographic separation such as reverse-phase ion pair (IPRP), anion exchange (AEX) and affinity chromatography (AC) using poly(dT) capture (Figure 3) efficiently purifies the mRNA target and removes the DNA template, eliminating the need for DNA digestion1, 3. Chromatography is also used after enzymatic capping to remove unwanted mRNA transcripts and oligonucleotide impurities.
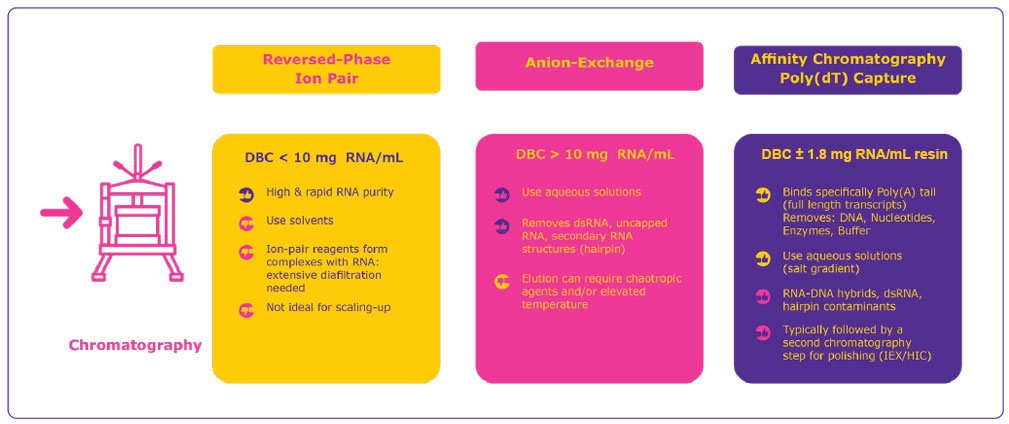
Figure 3:Comparison of reversed-phase ion-pair, anion exchange and affinity chromatography for mRNA purification (DBC: dynamic binding capacity).4,5
- Reverse-phase ion pairing (IPRP)can be used at small scales to efficiently capture the target single stranded RNA (ssRNA) and separate it from impurities. However, as this method requires solvents it is less suitable for GMP manufacturing and is better suited for polishing than for capture.
- Anion exchange (AEX) chromatography has a high dynamic binding capacity and efficiently removes impurities such as dsRNA, uncapped RNA, RNA–DNA hybrids and other RNA structures such as hairpin mRNA. While AEX uses aqueous solutions, it requires potentially toxic chaotropic agents and operating temperatures of up to 85 °C to desorb large mRNA molecules bound to the resin.
- Affinity chromatography (AC) poly(dT) capture uses a resin to specifically capture the poly(A) tail of full-length mRNA transcripts. This method efficiently removes DNA, nucleotides, enzymes, buffer components and any other impurities that don’t have a poly(A) tail. For this reason, AC is commonly used for initial mRNA capture, followed by AEX for polishing.
- Final concentration and diafiltration is performed following the chromatography step(s) to maximize product purity and transfer the mRNA into the appropriate buffer for formulation or storage.
Scale-up Considerations
Single-use technologies offer scalability, adaptability and quality for manufacturers with a large pipeline of targets and are a key enabler of many mRNA GMP manufacturing processes. GMP manufacturing leverages the advantages of TFF or chromatography steps for efficient large-scale separation, replacing alternative purification methods typical of process development at small scale. Considerations to keep in mind include:
- TFF or chromatography steps replace solvent extraction and precipitation steps frequently used in mRNA process development.
- High quality chemicals and endonuclease free reagents must be used wherever possible to improve mRNA stability and minimize the possibility of mRNA degradation.
Recent years have seen major successes in the roll out of mRNA vaccines to large patient populations. Although challenges remain, the focus on maximizing mRNA stability by using high quality chemicals and endonuclease free reagents, optimizing and tailoring chromatographic purification technologies to maximize separation and streamline scale-up, has resulted in major progress in GMP manufacturing templates.
To ensure mRNA technology reaches its full potential, innovative solutions, expertise and ingenuity will be needed to ensure robust platforms evolve at production scale. With our products, services and technical expertise, we are committed to developing integrated solutions to streamline your mRNA manufacturing.