L-半胱氨酸在细胞培养中的应用
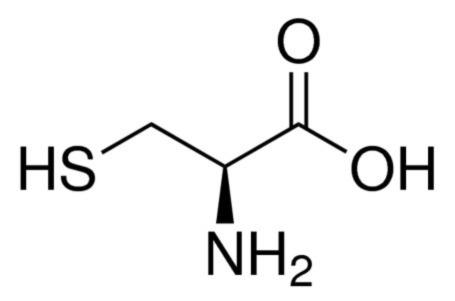
图1:L-半胱氨酸化学结构
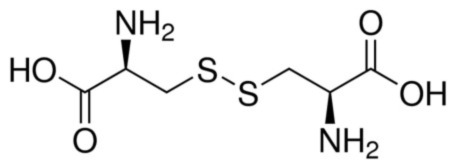
图2:L-胱氨酸化学结构
L-半胱氨酸在细胞培养基中的应用
L-半胱氨酸体外氧化为L-胱氨酸相对容易。细胞培养基的性能和稳定性受其各种形式的比例影响。用于无血清培养的补充培养基也因 R 链而变得复杂。这些 R 链包含参与硫醇氧化、还原和自由基化学以及金属配位化学的硫原子。
培养基中的铜可能影响这些氨基酸的溶解度,形成细胞无法吸收的复合物。亚铜也可能将胱氨酸还原为半胱氨酸。
L-半胱氨酸已用于配制Coon改良版F-12培养基、L-15培养基、McCoy's 5A改良培养基、MCDB培养基、Ham F-10营养混合物、Ham F-12营养混合物、Kaighn改良版Ham F-12营养混合物 (F12K)、无血清/无蛋白质的杂交瘤培养基。当这些培养基液态储存时,L-半胱氨酸可转化为L-胱氨酸。在极端条件下,L-胱氨酸可进一步氧化。
Ames培养基、Eagle基础培养基 (BME)、Click培养基、杜氏改良Eagle培养基(DMEM)、Glascow改良Eagle培养基(GMEM)、Iscove改良杜氏培养基 (IMDM)、Eagle最低基础培养基(EMEM)、RPMI-1640和其他培养基。
此外,还可采用不同配比将其配制成DMEM/Ham's 营养混合物 F-12 (50:50)、培养基 199、NCTC 培养基、Waymouth 培养基 MB、Williams 培养基 E。用于生物制造和组织工程的培养基通常含有额外的 L-半胱氨酸等价物, 如N-乙酰半胱氨酸。
L-半胱氨酸与 L-胱氨酸的区别
半胱氨酸的化学式为C3H7O2NS,分子量为121.16。胱氨酸由两个二硫键连接的半胱氨酸分子组成。它的化学式为C6H12O4N2S2,分子量为240.31。在细胞中,这两种分子都含有硫原子,为氧化还原活性和电子转移提供了位点。
半胱氨酸和胱氨酸通过不同的转运蛋白进入细胞,这有助于特定细胞控制各种形式的 L-半胱氨酸的利用方式。 此类形式包括L-半胱氨酸、L-胱氨酸、N-乙酰半胱氨酸(NAC)、混合二硫化物或者各种肽。除了它在蛋白质合成中的作用外,半胱氨酸还具有三肽谷胱甘肽的功能活性。
半胱氨酸还具有保护细胞免受氧化应激的重要间接作用。它是用于合成三肽谷胱甘肽的限速氨基酸。谷胱甘肽是参与阻断脂质过氧化和脱氢抗坏血酸氧化的主要水性抗氧化剂。在没有 L-半胱氨酸或其等价物的情况下,谷胱甘肽会迅速耗尽,细胞随即死亡
L-半胱氨酸和 L-胱氨酸在细胞中的主要功能
从营养学上来说,胱氨酸和半胱氨酸被认为是非必需氨基酸,因为它们可在哺乳动物的肝脏中合成。但是,对于细胞培养而言,它们是必须从外源提供的必需氨基酸。针对细胞自行配制有效培养基过程很复杂,因为这两种氨基酸之间可非酶促相互转化且不稳定。
胱氨酸残基是由蛋白质中的半胱氨酸巯基氧化形成的。蛋白质内和蛋白质间二硫键的形成和破坏在二级和三级结构的决定中起着重要作用。因此,这种氧化会影响细胞内蛋白质的结构。
许多细胞还可以代谢半胱氨酸,形成亚牛磺酸和牛磺酸。这两种分子分别通过与羟基自由基和次氯酸反应来帮助细胞培养基解毒。
半胱氨酸还可以参与蛋白质合成、自氧化、谷胱甘肽合成和辅酶A合成。了解它们的化学性质以及被细胞利用的方式是成功设计培养基的关键因素。
半胱氨酸和胱氨酸自由基化学
在体外,半胱氨酸易溶且最初以中性氨基酸存在。这种成分很不稳定,会发生非酶促自动氧化,而铁和/或铜阳离子会加速这种自动氧化。这些还原的阳离子与氨基酸络合,催化过氧化氢转化为羟基自由基和硫化物自由基。
半胱氨酸氧化受过渡金属铜和铁的影响很大。一价半胱氨酸氧化产生硫自由基。该自由基可以参与与双分子氧、另一个半胱氨酸硫基自由基(形成胱氨酸)或其他自由基的反应,传播氧化过程。
当半胱氨酸硫基与另一个硫基自由基反应时,自由基传播终止。胱氨酸易于进一步氧化,形成磺基丙氨酸和其他氧化产物。胱氨酸自由基还可与过氧化氢反应形成羟自由基。
所述反应可使胱氨酸和半胱氨酸无法供细胞使用或对细胞培养基产生毒性。了解它们的比例和数量很重要。细胞类型不同,摄取这两种氨基酸的能力也不同。