Viral Vector Vaccine Mfg
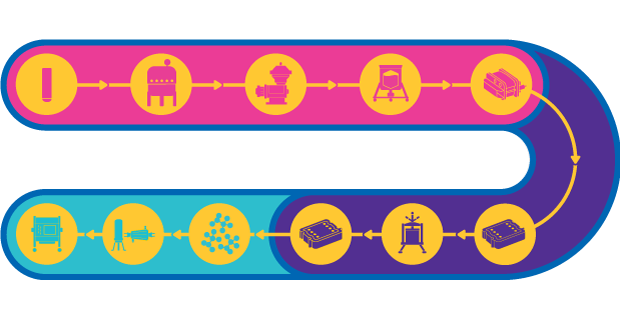
Process Train for Viral Vector Vaccines
A live vector vaccine uses an attenuated or harmless microorganism such as an adenovirus to transport portions of an antigen to stimulate an immune response. Vectored vaccines are capable of inducing potent cell-mediated immunity, which is essential for complex disease like AIDS, malaria, and cancer among others.
While the manufacturing process for vaccine vectors is fairly templated, some challenges may arise, since several different viruses with varying properties can be used. For large viral vectors, process sterility is critical due to yield loss associated with sterile filtration. There are also challenges with vector aggregation and stability.
In addition, many Phase I/II processes involve adherent cell cultures; as a result, scaling to Phase III and commercial manufacturing can require process adjustments to achieve production targets. In later phases, product yield and purity are critical, as high dosage titers are required in the final product. Learn more about viral vector vaccine manufacturing.
Featured Categories
The Mobius® Bioreactor family offers single-use bioreactors for cell culturing from early development to commercial production, supporting various scales.
Explore Mobius® single-use mixing solutions for pharmaceutical ingredient blending and process solution preparation.
Whether you are developing solutions, emulsions or suspensions – we provide high-quality pharmaceutical excipients for liquid formulations.
Our off-the-shelf and customizable bioprocessing cell culture media (CCM) products enhance productivity in upstream mAb, vaccine, gene/cell therapy processes.
Accelerate Time to Clinical While Ensuring Reliable Scale-up
Upstream culture processes developed for manufacturing of viral vector vaccines must be optimized to meet productivity requirements. This optimization includes the cell lysis and clarification steps which are essential for removal of cells and cell debris and to ensure a robust vector harvest. The upstream process is only successful, however, if it can be reliably scaled in order to meet anticipated market demand.
Achieve Yield and Efficiency Goals with Robust Impurity Removal
Nucleic acids from lysed cells are a common contaminant in viral vector vaccine processes. Regulations require that the level of carry-over host cell nucleic acid be below 10 ng/dose of attenuated viral vaccine. Benzonase® endonuclease treatment followed by tangential flow filtration is a robust and powerful combination to degrade and remove residual nucleic acid components.
Maximize Downstream Recovery
Small-scale clinical lots are typically purified using CsCl-based density gradient ultracentrifugation, while large-scale production requires a two- or three-step chromatography process. Anion exchange is typically used to remove HCP, DNA, RNA, and other major contaminants, while size exclusion chromatography is used for trace contaminant removal.
Ensure Patient Safety
Sterile filtration ensures the sterility of the final formulated product and patient safety. A filter pore size of 0.22 µm or less is required to eliminate microbial contaminants. A key consideration for the sterile filtration process is the level of viral aggregates. These aggregates need to be controlled by optimizing the formulation, otherwise, the sterile filtration process will be challenging with the potential for high losses in yield.
Nuclease Treatment & Clarification
Ensure robust scalability.
- Nuclease Treatment with Benzonase® Suitable for Biopharmaceutical Production EMPROVE® Bio
- Benzonase® Detection with Benzonase® Elisa Kit II to Detect Left Over Benzonase® Endonuclease in the Process
- Primary/Secondary Clarification with Millistak+® HC POD Depth Filters
- Primary Clarification with Clarisolve® Depth Filters
- Clarification Depth Filters & Pretreatment Solutions
- Clarification with Milligard® PES filters
Downstream - Tangential Flow Filtration
Achieve yield, efficiency and pDNA recovery goals while ensuring robust impurity removal.
- Ultrafiltration / Diafiltration with Pellicon® 2 Cassettes
- Ultrafiltration / Diafiltration with Pellicon® 3 Cassettes
- Ultrafiltration / Diafiltration with Pellicon® Capsule with Ultracel® Membrane
- Mobius® TFF 80 System, Mobius® FlexReady Solution for TFF, Cogent® Lab Systems and Cogent® Process-scale Tangential Flow Filtration System
Downstream Chromatography
- Membrane Chromatography with Eshmuno® Q Resin
- Membrane Chromatography with Natrix® Q Recon Mini Chromatography Membranes
- Membrane Chromatography with Natrix® Q Pilot Chromatography Membrane
- Membrane Chromatography with Natrix® Q Recon Mini
- Membrane Chromatography with Eshmuno® Q Resin
- Capture and/or Polishing Chromatography with Fractogel® EMD DEAE Chromatography Resins
- Capture and/or Polishing Chromatography with Fractogel® EMD DMAE Chromatography Resins
- Mobius® FlexReady Solution for Chromatography

Downstream Process Chemicals and Formulation
Bioprocessing Liquid Cell Culture Media & Buffers
We offer the industry’s highest quality sterile filtered liquid capabilities, supplying ready-to-use cell culture media, buffers, CIP and SIP products from GMP facilities worldwide to optimize your biopharma production.
Final Sterile Filtration & Filling
Ensure patient safety with a reliable and robust sterile filtration process.
Analytics Software & PAT Technology
Visit our document search for data sheets, certificates and technical documentation.
Related Articles
- Cost Modeling Vaccine Manufacturing: Estimate Production Costs for mRNA and other Vaccine ModalitiesA custom-designed cost model is used to explore the economics of vaccine manufacturing across several different modalities including mRNA. The model enables greater process understanding, simulates bottlenecks, and helps to optimize production efficiency.
- This technical article breaks down the adenovirus vaccine manufacturing process and provides a case study on developing an accelerated and cost-effective single-use adenoviral vector vaccine.
- This page shows how to purify or remove viruses with a Capto DeVirS, AVB Sepharose High Performance from Cytiva.
- Method development for protein fingerprinting of AAV serotype 5 using both intact mass analysis and peptide mapping, to determine critical quality attributes for gene therapy, utilizing three different columns.
- Upstream gene therapy optimization maximizes viral vector titers; partner with technology experts for HEK293, HEK293T, and Sf9 cell solutions.
- See All (3)
Find More Articles and Protocols
How Can We Help
In case of any questions, please submit a customer support request
or talk to our customer service team:
Email custserv@sial.com
or call +1 (800) 244-1173
Additional Support
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- Calculators & Apps
Web Toolbox - science research tools and resources for analytical chemistry, life science, chemical synthesis and materials science.
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
To continue reading please sign in or create an account.
Don't Have An Account?