顶空级溶剂在有机挥发性杂质分析之中的应用
简介
在制药制剂合成和生产步骤之中,有时仍存在有机挥发性杂质(OVI)残留问题。出于健康和安全原因,须检验确保这类溶剂未超过美国药典(USP)和国际协调会(ICH)指南(1,2)规定的浓度限制。静态顶空液相色谱(SH-GC)是分析这类OVI常用的技术。该技术可浓缩挥发性分析物,其无样品基质的情况下进行分析。
SH-GC分析样品必须溶解在适宜的溶剂中;除溶解样品外,所选溶剂还必须对顶空目标分析物具有充分的灵敏度。分配系数会影响分析物从液体样品进入顶空的能力,数值越低,蒸气压越高,顶空灵敏度越高(3)。因此,对于低含量检测,目标分析物在所选溶剂中的分配系数必须足够低。此外,溶剂本身的蒸气压应足够低,以免“溢流”顶空而影响OVI分析物检测。
水具有超低的分析物分配系数且蒸气压较低,但并非在所有情况下均适用。USP <467>和欧洲药典(EP)各论列出了水溶性和水不溶性样品的操作程序。对于水不溶性样品,USP <467>指定使用二甲基亚砜(DMSO)和二甲基甲酰胺(DMF)溶剂。其他经证适合水不溶性样品顶空分析的溶剂包括二甲基乙酰胺(DMAC)和1,3-二甲基-2-咪唑啉酮(DMI),稍后将在EP方法2.4.24 (4)中详述。在色谱分析时,这类溶剂迟于大多数OVI分析物洗脱,且蒸气压远远低于许多其他高沸点有机化合物。
为避免色谱分析出现多余的峰并干扰目标分析物,溶剂纯度至关重要。许多进行OVI分析的实验室遵循的实验方案都要求分析允许的空白样,某些公开的方法(例如EP方法2.4.24)要求分析空白样以验证是否存在干扰峰。我们现在可提供经过专门检验、保证适于SH-GC分析的高纯度顶空级溶剂。
实验
本实验评估了DMSO顶空级溶剂在SH-GC分析OVI中的应用。使用顶空级和其他等级的DMSO制备空白样,评估顶空溶剂纯度。然后将空白样中的峰保留时间与顶空级DMSO溶剂制得的OVI标准品进行比较。
将1 mL DMSO吸取到10 mL顶空瓶中制备空白样,针对密封瓶进行SH-GC分析。OVI工作标准品包括多种常见工艺溶剂,代表了USP <467>和ICH指南规定的不同类别。这类标准品采用顶空级DMSO稀释DMAC储备溶液制得。表1总结了OVI工作标准品的组分和终浓度。以与空白样类似的方式制备SH-GC分析工作标准品。使用表2中列出的参数SH-GC分析空白样和标准品。
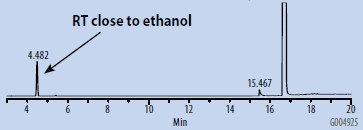
图 1.SH-GC空白样,DMSO - 有机合成级
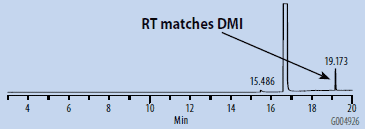
图 2.SH-GC空白样,DMSO - 顶空级
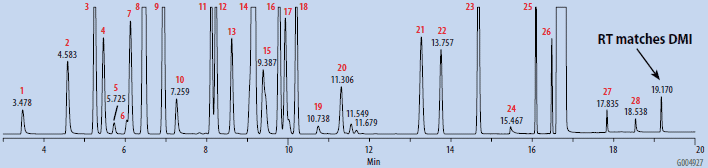
图 3.SH-GC分析采用顶空级DMSO制备的OVI工作标准品